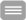Jena (UKJ) Sie bilden ein auffälliges Muster in der Struktur Tausender Proteine, die in den verschiedensten Arten von Lebewesen vorkommen – wiederholte Faltungen (repeats) von bestimmten Aminosäureabfolgen, die einen leicht gekrümmten Stapel bilden. Diese Ankyrin repeats, die nach Proteinen im Zellskelett benannt sind, wurden bereits vor 40 Jahren als generelles Strukturelement identifiziert. Proteine mit diesem Strukturmuster wurden als Signalproteine in wichtigen Zell- und auch Krankheitsprozessen beschrieben. Bislang war es jedoch noch nicht gelungen, diesen Strukturen eine allgemeine Funktion zuzuordnen.
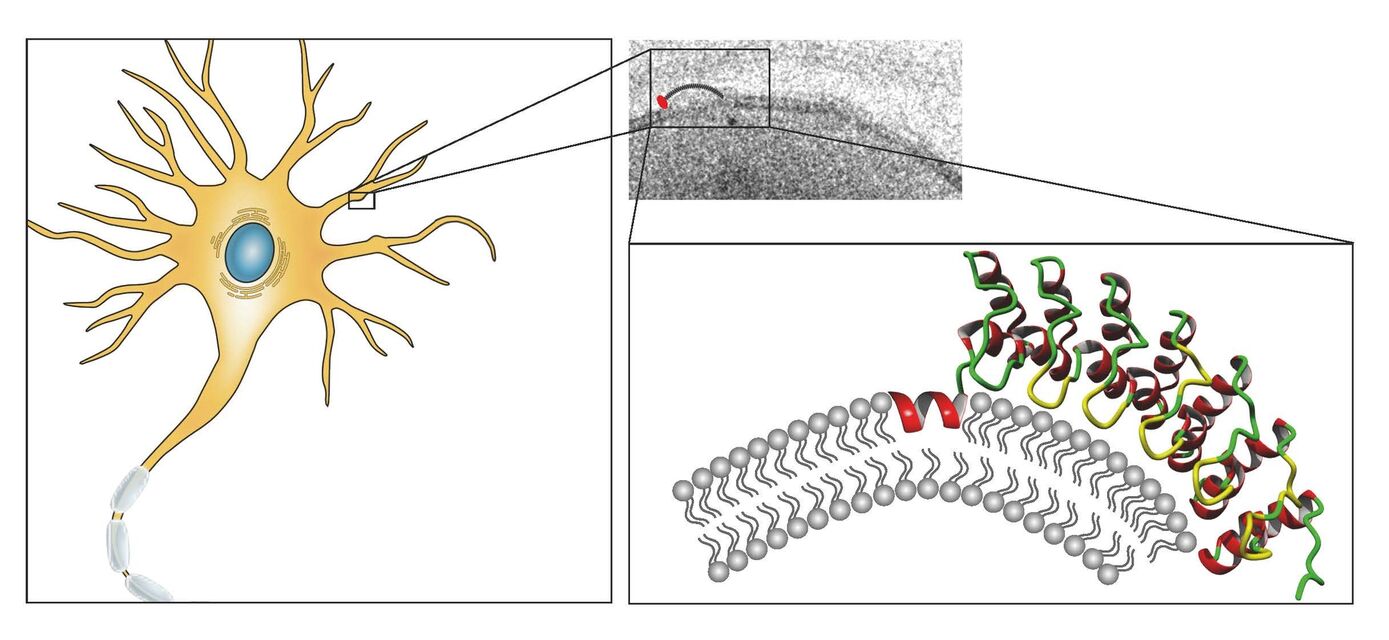
Bei ihren Analysen des Proteins Ankycorbin, das unter anderem in Nervenzellen vorkommt, nahmen Wissenschaftler und Wissenschaftlerinnen am Universitätsklinikum Jena speziell die Ankyrin repeats ins Visier und untersuchten deren biochemische und zellbiologische Funktionen. Ihre Ergebnisse veröffentlichten die Autoren um die Biochemikerin Prof. Dr. Britta Qualmann und den Biochemiker PD Dr. Michael Kessels jetzt im Fachjournal Nature Cell Biology. „Wir hatten die Vermutung, dass wir es bei Ankycorbin mit einem Zellmembran-krümmenden Protein zu tun haben könnten. Derartige Proteine können für spezifische Gestaltgebungen von Zellen innerhalb von Geweben und Organen von großer Wichtigkeit sein. Also sind wir dieser Hypothese experimentell nachgegangen“, beschreibt PD Dr. Michael Kessels den Ausgangspunkt der Studie.
Ankycorbin krümmt Membranen
Dazu testeten die Wissenschaftler und Wissenschaftlerinnen Ankycorbin auf drei wesentliche Eigenschaften: Zunächst wiesen sie mit verschiedenen Methoden nach, dass das Protein überhaupt an Membranen binden kann. Dann müssen Membrankrümmungsproteine über eine ausgedehnte gekrümmte Bindungsfläche verfügen – mit den leicht gebogenen Ankyrin repeats ist Ankycorbin dafür bestens ausgestattet und bevorzugte in der Tat gekrümmte Membranen. Mittels hochauflösender, elektronenmikroskopischer Analysen von sich entwickelnden Neuronen konnten die Wissenschaftler schließlich auch zeigen, dass das Protein an Nervenzellmembranen größere Überstrukturen bildet. Biochemisch konnte nachgewiesen werden, dass sich mehrere Moleküle Ankycorbin zusammenlagern können. Dadurch kann eine Krümmung der Membran über einen größeren Bereich fortgesetzt werden. Interessanterweise traten solche Ankycorbin-Cluster vorwiegend an eng umgrenzten, auswärts gekrümmten Membranarealen auf.
Dass Ankycorbin nicht nur die Voraussetzungen erfüllt, sondern tatsächlich Membranen krümmen kann, wiesen dann weitere biochemische Arbeiten nach. „Allerdings zeigte sich, dass zwar die grundlegende Idee stimmte, die Ankyrin repeats aber eher für Proteinlagerungen passende Membrankrümmungen erkannten statt solche Krümmungen aktiv zu erzwingen – das machte tatsächlich eine benachbarte helikale Struktur, die sich wie ein Keil in Membranen hineinzwängen kann, und so die eigentliche Arbeit bei der festen Bindung und bei der Membrankrümmung leistet. Diese neuartige Kombination von miteinander arbeitenden Strukturen haben wir dann N-Ank-Modul genannt“, so Britta Qualmann.
Ankycorbin ist bei der Gestaltausbildung von Nervenzellen wichtig
Wie Ankycorbin auf molekularer Ebene agiert, war nun geklärt, aber die Wissenschaftler wollten auch die Funktion im Organismus verstehen. „Wir hatten festgestellt, dass Ankycorbin im Gehirn vor allem vor der Geburt vorkommt, der Gehalt dann aber abfällt. Das deutete auf eine mögliche Rolle in frühen Entwicklungsprozessen von Nervenzellen hin“, so Michael Kessels. Und tatsächlich hatte es dramatische Auswirkungen, wenn den Nervenzellen Ankycorbin fehlte. Die Ausläufer und deren Verzweigungen, mit denen Nerventellen Signale aufnehmen und weiterleiten, die sogenannten Dendriten, blieben unterentwickelt. In systematischen Versuchen mit veränderten Ankycorbin-Proteinen wiesen die Wissenschaftler nach, dass sowohl die Ankyrin repeats, die sich in die Membran hineinzwängende Keilstruktur als auch die Fähigkeit zur Zusammenlagerung für die Funktion von Ankycorbin in der Ausbildung normalgestalteter Nervenzellen notwendig sind.
Ankycorbin als Mitglied einer neuen Protein-Superfamilie
Die Biochemiker und Biochemikerinnen in Jena sind dann noch einen Schritt weitergegangen und haben untersucht, ob Ankycorbin ein allgemeineres Struktur-Funktionsprinzip repräsentiert. Dazu durchforsteten sie die Genome verschiedener Arten nach strukturell verwandten Proteinen und testeten diese auf ihre Fähigkeit zur Membranbindung und -krümmung. Mit Erfolg: Sie konnten schließlich eine ganze Superfamilie ähnlich funktionierender Proteine etablieren. „Wir haben da wirklich eine neue Tür aufgestoßen. Es ist jetzt sehr spannend herauszufinden, wie all die neu gefundenen N-Ank-Proteine Membranen binden und krümmen - und welche biologische Funktionen in unserem Körper sie damit übernehmen. Da werden wir sicher noch einige Überraschungen erleben“, so Britta Qualmann.
Originalliteratur:
Wolf et. al. Ankyrin repeat-containing N-Ank proteins shape cellular membranes. Nature Cell Biology, 2019, doi: 10.1038/s41556-019-0381-7
Kontakt:
Prof. Dr. Britta Qualmann & PD Dr. Michael Kessels
Institut für Biochemie I, Universitätsklinikum Jena
Tel. 03641/ 9 396 310
E-Mail: ,